نمونه هایی از واکنش های شیمیایی در زندگی روزمره

شیمی تنها محدود به آزمایشگاه ها نیست؛ این علم در زندگی روزمره ما جریان دارد و هر روز شاهد واکنش های شیمیایی مختلفی هستیم که دنیای اطراف ما را شکل می دهند. از پختن غذا تا تنفس، از سوختن شمع تا زنگ زدن فلزات، همه این ها نمونه هایی از واکنش های شیمیایی هستند که به طور مداوم در حال وقوع اند. در این مقاله، به بررسی برخی از این واکنش ها می پردازیم و نشان می دهیم که چگونه شیمی در زندگی روزمره ما نقش اساسی ایفا می کند.
فرآیند فتوسنتز در گیاهان

Frank Krahmer / Getty Images
فتوسنتز یکی از مهم ترین واکنش های شیمیایی در طبیعت است که توسط گیاهان انجام می شود. در این فرآیند، گیاهان با استفاده از نور خورشید، دی اکسید کربن و آب، غذا (گلوکز) و اکسیژن تولید می کنند. این واکنش نه تنها برای رشد و بقای گیاهان ضروری است، بلکه نقش حیاتی در تولید اکسیژن مورد نیاز برای تنفس موجودات زنده نیز دارد. معادله شیمیایی فتوسنتز به این صورت است:
6 CO2 + 6 H2O + نور → C6H12O6 + 6 O2
این فرآیند به عنوان یکی از پایه های حیات روی زمین شناخته می شود و بدون آن، چرخه حیات به طور کامل مختل می شد.
تنفس سلولی هوازی و بی هوازی
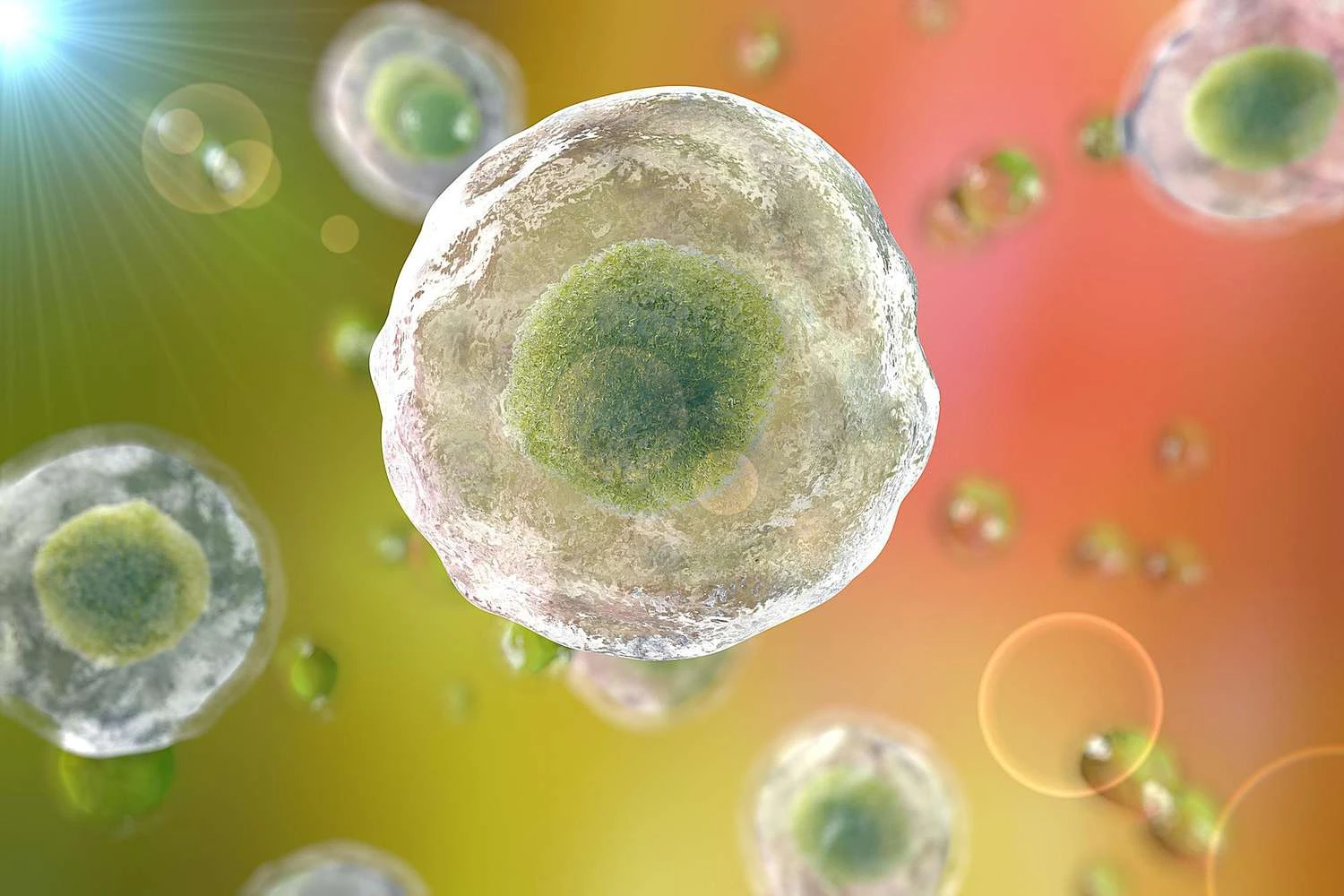
Kateryna Kon/Science Photo Library / Getty Images
تنفس سلولی فرآیندی است که در آن سلول های بدن انرژی مورد نیاز خود را از طریق تجزیه مولکول های غذایی به دست می آورند. این فرآیند به دو شکل هوازی و بی هوازی انجام می شود. در تنفس هوازی، سلول ها از اکسیژن برای تجزیه گلوکز استفاده می کنند و در نتیجه، انرژی، دی اکسید کربن و آب تولید می شود. معادله کلی این واکنش به این صورت است:
C6H12O6 + 6O2 → 6CO2 + 6H2O + انرژی (36 ATP)
در مقابل، تنفس بی هوازی در شرایطی اتفاق می افتد که اکسیژن کافی در دسترس نباشد، مانند فعالیت های ورزشی شدید. در این حالت، سلول ها از روش های دیگری برای تولید انرژی استفاده می کنند که منجر به تولید موادی مانند اسید لاکتیک یا اتانول می شود. معادله کلی یکی از انواع تنفس بی هوازی به این شکل است:
C6H12O6 → 2C2H5OH + 2CO2 + انرژی
این فرآیندها نه تنها در بدن انسان، بلکه در تولید محصولاتی مانند ماست، نان و شراب نیز نقش دارند.
سوختن و احتراق

سوختن یکی از رایج ترین واکنش های شیمیایی است که در زندگی روزمره با آن مواجه می شویم. این فرآیند زمانی اتفاق می افتد که یک ماده سوختنی با اکسیژن ترکیب شده و انرژی، دی اکسید کربن و آب تولید می کند. نمونه های آشنا شامل روشن کردن کبریت، سوختن شمع یا روشن کردن آتش است. معادله کلی سوختن پروپان، که در کباب پزها و برخی شومینه ها استفاده می شود، به این صورت است:
C3H8 + 5O2 → 4H2O + 3CO2 + انرژی
این واکنش نه تنها گرما و نور تولید می کند، بلکه در صنعت و زندگی روزمره نیز کاربردهای گسترده ای دارد. سوختن به عنوان یک واکنش اکسیداسیون سریع شناخته می شود و نقش مهمی در تولید انرژی و گرمایش ایفا می کند.
زنگ زدن فلزات

Alex Dowden/EyeEm / Getty Images
زنگ زدن فلزات، به ویژه آهن، یک نمونه رایج از واکنش های اکسیداسیون در زندگی روزمره است. این فرآیند زمانی اتفاق می افتد که آهن با اکسیژن و رطوبت موجود در هوا واکنش داده و اکسید آهن (زنگ) تشکیل می دهد. این واکنش نه تنها باعث تغییر رنگ فلز به قرمز یا نارنجی می شود، بلکه به مرور زمان باعث تخریب ساختار فلز نیز می گردد. معادله شیمیایی زنگ زدن آهن به این صورت است:
Fe + O2 + H2O → Fe2O3.XH2O
زنگ زدن تنها محدود به آهن نیست؛ فلزات دیگری مانند مس نیز در معرض اکسیداسیون قرار می گیرند و لایه هایی مانند زنگار (وردیگریس) روی سطح آن ها تشکیل می شود. این پدیده در صنعت و زندگی روزمره اهمیت زیادی دارد، زیرا باعث کاهش دوام و مقاومت فلزات می شود و نیاز به روش های محافظتی مانند رنگ آمیزی یا استفاده از روکش های ضد زنگ را افزایش می دهد.
واکنش های جابجایی دوگانه

واکنش های جابجایی دوگانه، که به آن ها واکنش های متاتزیس نیز گفته می شود، نوعی از واکنش های شیمیایی هستند که در آن دو ترکیب شیمیایی با یکدیگر واکنش داده و یون های خود را جابجا می کنند. این واکنش ها معمولاً منجر به تشکیل ترکیبات جدیدی مانند گاز، آب یا رسوب می شوند. یک مثال آشنا از این واکنش، ترکیب سرکه (اسید استیک) و جوش شیرین (بی کربنات سدیم) است که در نتیجه آن گاز دی اکسید کربن و آب تولید می شود. معادله شیمیایی این واکنش به این صورت است:
HC2H3O2(aq) + NaHCO3(aq) → NaC2H3O2(aq) + H2O(l) + CO2(g)
این نوع واکنش ها نه تنها در آزمایش های علمی مانند آتشفشان شیمیایی کاربرد دارند، بلکه در پخت و پز نیز نقش مهمی ایفا می کنند. برای مثال، در تهیه نان و کیک، گاز دی اکسید کربن تولید شده باعث پف کردن و سبک شدن محصول نهایی می شود.
الکتروشیمی و باتری ها

الکتروشیمی شاخه ای از علم شیمی است که به مطالعه واکنش های شیمیایی می پردازد که در آن ها انرژی شیمیایی به انرژی الکتریکی تبدیل می شود یا برعکس. این فرآیندها پایه ی عملکرد باتری ها هستند. در باتری ها، واکنش های اکسیداسیون و کاهش (ردوکس) به طور خودبه خودی یا غیرخودبه خودی اتفاق می افتند و انرژی شیمیایی را به شکل جریان الکتریکی در دسترس قرار می دهند.
به عنوان مثال، در باتری های معمولی مانند باتری قلمی، واکنش های شیمیایی بین مواد داخل باتری باعث تولید الکترون ها می شود که از طریق مدار خارجی جریان می یابند و انرژی مورد نیاز دستگاه ها را تأمین می کنند. این فرآیندها نه تنها در باتری های خانگی، بلکه در باتری های خودروهای الکتریکی و سیستم های ذخیره سازی انرژی نیز کاربرد گسترده ای دارند.
الکتروشیمی همچنین در فرآیندهایی مانند آبکاری فلزات و تولید مواد شیمیایی خاص نیز استفاده می شود و نقش مهمی در صنعت و فناوری های نوین ایفا می کند.
هضم غذا و واکنش های آنزیمی

Peter Dazeley/Photographer's Choice / Getty Images
هضم غذا فرآیندی پیچیده است که در آن هزاران واکنش شیمیایی به کمک آنزیم ها انجام می شود. این فرآیند از دهان آغاز می شود، جایی که آنزیم هایی مانند آمیلاز موجود در بزاق شروع به تجزیه کربوهیدرات ها به قندهای ساده تر می کنند. با ورود غذا به معده، اسید هیدروکلریک و آنزیم های گوارشی مانند پپسین به تجزیه پروتئین ها و چربی ها کمک می کنند.
در روده ها، آنزیم های بیشتری مانند لیپاز و پروتئاز به کار گرفته می شوند تا مواد غذایی را به مولکول های کوچک تری تبدیل کنند که بتوانند از دیواره روده جذب شده و وارد جریان خون شوند. این مولکول ها سپس به سلول های بدن منتقل می شوند تا به عنوان منبع انرژی یا مواد ساختمانی مورد استفاده قرار گیرند.
بدون این واکنش های آنزیمی، بدن قادر به جذب مواد مغذی ضروری نخواهد بود و عملکرد طبیعی آن مختل می شود. بنابراین، هضم غذا نه تنها یک فرآیند مکانیکی، بلکه یک فرآیند شیمیایی حیاتی است که به بدن امکان می دهد از مواد غذایی استفاده کند.
واکنش های اسید و باز

Lumina Imaging / Getty Images
واکنش های اسید و باز از رایج ترین واکنش های شیمیایی در زندگی روزمره هستند. در این واکنش ها، یک اسید و یک باز با یکدیگر ترکیب می شوند و نمک و آب تولید می کنند. این فرآیند به عنوان خنثی سازی شناخته می شود. برای مثال، ترکیب سرکه (یک اسید ضعیف) با جوش شیرین (یک باز) منجر به تولید نمک، آب و گاز دی اکسید کربن می شود.
معادله کلی یک واکنش اسید و باز به این صورت است:
HCl + NaOH → NaCl + H2O
این واکنش ها نه تنها در آزمایش های شیمیایی، بلکه در صنعت و زندگی روزمره نیز کاربردهای فراوانی دارند. برای مثال، در تولید مواد شوینده، تنظیم pH خاک در کشاورزی و حتی در پزشکی برای درمان برخی مشکلات معده استفاده می شوند. درک این واکنش ها به ما کمک می کند تا از مواد شیمیایی به طور ایمن و مؤثر استفاده کنیم.
واکنش های صابون و مواد شوینده

JGI/Jamie Grill / Getty Images
صابون و مواد شوینده از طریق واکنش های شیمیایی خاصی عمل می کنند که به آن ها امکان می دهد چربی ها و آلودگی ها را از سطوح جدا کنند. صابون ها از طریق فرآیندی به نام صابونی سازی تولید می شوند که در آن چربی ها یا روغن ها با یک باز قوی مانند سدیم هیدروکسید واکنش می دهند. این واکنش منجر به تشکیل صابون و گلیسرول می شود.
صابون ها مولکول هایی با دو بخش آبدوست (جذب کننده آب) و آبگریز (جذب کننده چربی) هستند. بخش آبگریز به چربی ها می چسبد، در حالی که بخش آبدوست به آب متصل می شود. این ویژگی باعث می شود چربی ها از سطوح جدا شده و به راحتی با آب شسته شوند.
مواد شوینده نیز به طور مشابه عمل می کنند، اما ساختار شیمیایی آن ها به گونه ای است که در آب سخت نیز مؤثر هستند. این مواد با کاهش کشش سطحی آب، به نفوذ بهتر آن به داخل الیاف و جدا کردن آلودگی ها کمک می کنند. این واکنش ها نه تنها در شست وشوی لباس ها، بلکه در تمیز کردن سطوح مختلف نیز کاربرد دارند.
تغییرات شیمیایی در پخت و پز

پخت و پز یکی از رایج ترین فعالیت هایی است که در آن تغییرات شیمیایی به وضوح دیده می شود. این تغییرات نه تنها طعم و بافت غذا را بهبود می بخشند، بلکه مواد غذایی را برای هضم آسان تر آماده می کنند. برای مثال، هنگام پختن تخم مرغ، پروتئین های موجود در سفیده و زرده تخم مرغ دچار تغییر ساختار می شوند و از حالت مایع به جامد تبدیل می شوند. این فرآیند به نام دناتوره شدن پروتئین شناخته می شود.
یکی دیگر از واکنش های مهم در پخت و پز، واکنش میلارد است. این واکنش زمانی اتفاق می افتد که آمینواسیدها و قندها در دمای بالا با یکدیگر واکنش داده و ترکیبات جدیدی ایجاد می کنند که باعث تغییر رنگ و طعم غذا می شوند. این واکنش در برشته کردن نان، سرخ کردن گوشت و حتی پختن قهوه نقش دارد.
تغییرات شیمیایی در پخت و پز نه تنها غذا را خوش طعم تر می کنند، بلکه ارزش غذایی آن را نیز تحت تأثیر قرار می دهند. درک این فرآیندها به ما کمک می کند تا غذاها را به شیوه ای سالم تر و مؤثرتر آماده کنیم.
- شیمی
- علم



