فلزات و غیرفلزات: تفاوت ها و ویژگی های اصلی آن ها
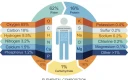
عناصر را می توان براساس خواصشان به فلزات و غیرفلزات تقسیم بندی کرد. اغلب اوقات، با نگاه کردن به درخشش فلزی یک عنصر می توانید تشخیص دهید که آن یک فلز است، اما این تنها تفاوت بین فلزات و غیرفلزات نیست.
نکات کلیدی: تفاوت بین فلزات و غیرفلزات
- جدول تناوبی شامل عناصری است که فلزات هستند، عناصری که غیرفلزات هستند و عناصری با خواص میان تهی بین این دو گروه (نیمه فلزات).
- فلزات معمولاً جامدات سخت و با ظاهر فلزی هستند و دارای مقادیر بالای هدایت الکتریکی و حرارتی و همچنین دماهای ذوب و جوش بالایی هستند.
- غیرفلزات معمولاً عناصری نرم تر و گاهی رنگی هستند. آن ها می توانند جامد، مایع یا گاز باشند. دماهای ذوب و جوش آن ها معمولاً پایین تر از اکثر فلزات است و معمولاً هدایت کننده های خوبی نیستند.
فلزات
اکثر عناصر فلز هستند. این شامل فلزات قلیایی، فلزات قلیایی خاکی، فلزات انتقالی، لانتانیدها و اک틴یدها می شود. در جدول تناوبی، فلزات از غیرفلزات با خطی زیک زاک تفکیک شده اند که از کربن، فسفر، سلنیوم، ید و رادون عبور می کند. این عناصر و آن هایی که در سمت راست آن ها قرار دارند، غیرفلزات هستند. عناصر درست در سمت چپ این خط می توانند به عنوان نیمه فلزات یا نیمه عناصر نامیده شوند و خواص میان تهی بین فلزات و غیرفلزات را دارند. خواص فیزیکی و شیمیایی این عناصر را می توان مشاهده کرد تا تفاوت بین فلزات و غیرفلزات مشخص شود.
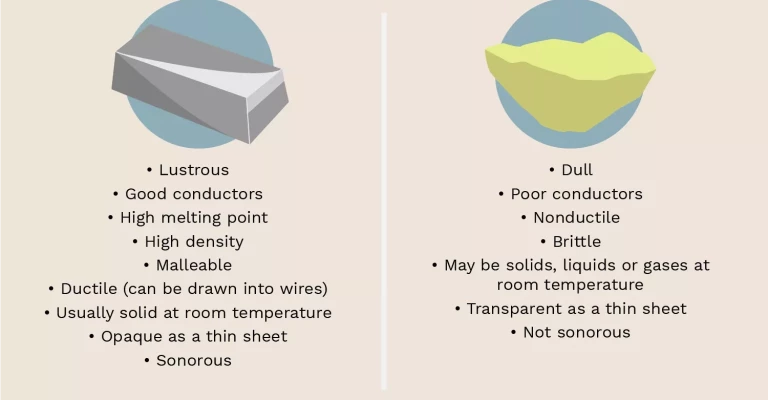
خواص فیزیکی فلزات:
- درخشان (براق)
- هدایت کننده های خوب حرارت و برق
- دمای ذوب بالا
- چگالی بالا (سنگین نسبت به اندازه خود)
- قابل چکش کاری (می توانند به شکل ورق درآیند)
- قابل کشش (می توانند به سیم تبدیل شوند)
- معمولاً در دمای اتاق جامدند (مکثی وجود دارد: جیوه)
- به عنوان یک ورق نازک، اوپک هستند (نمی توان از فلزات دید)
- فلزات زنگ صدایی دارند یا هنگامی که ضربه می خورند، صدای چنگ مانند تولید می کنند
خواص شیمیایی فلزات:
- هر اتم فلز ۱ تا ۳ الکترون در لایه خارجی خود دارد و به راحتی الکترون ها را از دست می دهد.
- به راحتی زنگ می زنند (مثلاً آسیب دیده از اکسیداسیون مثل تیرگی یا زنگ زدگی).
- به آسانی الکترون ها را از دست می دهند.
- اکسیدهایی که تشکیل می دهند، قلیایی هستند.
- الکترونگاتیویته کمتری دارند.
- عوامل کاهنده خوبی هستند.

فلز: مس (چپ)؛ نیمه فلز: آرسنیک (وسط) و غیرفلز: گوگرد (راست).
غیرفلزات
غیرفلزات، به استثنای هیدروژن، در سمت راست جدول تناوبی قرار دارند. عناصری که غیرفلز هستند شامل هیدروژن، کربن، نیتروژن، فسفر، اکسیژن، گوگرد، سلنیوم، تمام هالوژن ها و گازهای نجیب می باشند.
خواص فیزیکی غیرفلزات:
- بدون درخشندگی (ظاهر مات)
- هدایت کننده های ضعیف حرارت و برق
- جامدات غیرقابل کشش
- جامدات ترد
- ممکن است در دمای اتاق جامد، مایع یا گاز باشند.
- به عنوان یک ورق نازک، شفاف هستند.
- غیرفلزات صدای زنگ مانند تولید نمی کنند.
خواص شیمیایی غیرفلزات:
- معمولاً ۴ تا ۸ الکترون در لایه خارجی خود دارند.
- به راحتی الکترون های ظرفیت را به صورت اضافه یا مشترک می سازند.
- اکسیدهایی که تشکیل می دهند، اسیدی هستند.
- الکترونگاتیویته بالاتری دارند.
- عوامل اکسنده خوبی هستند.
هم فلزات و هم غیرفلزات اشکال مختلف (آلوتروپ ها) دارند که ظاهری و خواص متفاوت با یکدیگر دارند. برای مثال، گرافیت و الماس دو آلوتروپ از غیرفلز کربن هستند، در حالی که فریت و آستنیت دو آلوتروپ از آهن هستند. در حالی که غیرفلزات ممکن است آلوتروپی داشته باشند که ظاهری فلزی دارد، همه آلوتروپ های فلزات ظاهری دارند که ما آن را به عنوان یک فلز می شناسیم (درخشان و براق).
نیمه فلزات
تفاوت بین فلزات و غیرفلزات کمی مبهم است. عناصری که خواص هر دو گروه، یعنی فلزات و غیرفلزات را دارند، نیمه فلزات یا متالوئیدها نامیده می شوند. خطی که به صورت پله ای فلزات را از غیرفلزات در جدول تناوبی جدا می کند، به طور تقریبی این دو گروه را تفکیک می کند. اما شیمی دانان می دانند که نامیدن یک عنصر به عنوان "فلز" و عنصر کناری آن به عنوان "نیمه فلز" یک تصمیم قضاوتی است. در حقیقت، بیشتر فلزات تحت شرایط خاص خواص غیرفلزات را نشان می دهند و غیرفلزات در برخی شرایط مانند فلزات عمل می کنند.
هیدروژن یکی از نمونه های خوب عنصری است که گاهی به عنوان غیرفلز عمل می کند و گاهی به عنوان فلز. در شرایط عادی، هیدروژن یک گاز است و به همین دلیل مانند یک غیرفلز عمل می کند. اما تحت فشار بالا، به یک فلز جامد تبدیل می شود. حتی به عنوان یک گاز، هیدروژن اغلب کاتیون +1 را تشکیل می دهد (یک ویژگی فلزی). با این حال، گاهی اوقات آن آنیون -1 را تشکیل می دهد (ویژگی غیرفلزی).
- شیمی
- علم