تعریف و ویژگی های پیوند قطبی در شیمی
پیوندهای شیمیایی به دو دسته قطبی و غیرقطبی تقسیم می شوند. تفاوت آن ها در نحوه توزیع الکترون ها در پیوند است.
نکات کلیدی: پیوند قطبی در شیمی چیست؟
- پیوند قطبی نوعی پیوند کووالانسی است که در آن الکترون های تشکیل دهنده پیوند به طور نابرابر توزیع شده اند. به عبارت دیگر، الکترون ها بیشتر در یک سمت پیوند نسبت به سمت دیگر قرار دارند.
- پیوندهای قطبی در میان پیوندهای کووالانسی خالص و پیوندهای یونی قرار دارند. این پیوندها زمانی شکل می گیرند که تفاوت الکتروگاتیویته بین کاتیون و آنیون بین 0.4 و 1.7 باشد.
- نمونه هایی از مولکول هایی که دارای پیوندهای قطبی هستند شامل آب، هیدروژن فلوراید، دی اکسید گوگرد و آمونیاک می باشند.
تعریف پیوند قطبی
پیوند قطبی، پیوندی کووالانسی بین دو اتم است که در آن الکترون های تشکیل دهنده پیوند به طور نابرابر توزیع شده اند. این امر باعث می شود که مولکول دارای یک دیپول الکتریکی جزئی باشد که یک انتها کمی مثبت و انتهای دیگر کمی منفی است. بار دیپول های الکتریکی کمتر از بار کامل یک واحد است، بنابراین به عنوان بارهای جزئی در نظر گرفته می شوند و با دلتا مثبت (δ+) و دلتا منفی (δ-) نشان داده می شوند. به دلیل اینکه بارهای مثبت و منفی در پیوند جدا شده اند، مولکول های دارای پیوندهای کووالانسی قطبی با دیپول ها در مولکول های دیگر انترکشن می شوند. این منجر به نیروهای بین مولکولی دیپول-دیپول بین مولکول ها می گردد.
پیوندهای قطبی خط تفکیک بین پیوندهای کووالانسی خالص و پیوندهای یونی خالص هستند. پیوندهای کووالانسی خالص (پیوندهای غیرقطبی) جفت های الکترونی را به طور مساوی بین اتم ها تقسیم می کنند. از نظر فنی، پیوندهای غیرقطبی تنها زمانی رخ می دهند که اتم ها با یکدیگر یکسان باشند (به عنوان مثال، گاز H2)، اما شیمیدان ها هر پیوندی را که بین اتم ها با تفاوت الکتروگاتیویته کمتر از 0.4 باشد، به عنوان یک پیوند کووالانسی غیرقطبی در نظر می گیرند. دی اکسید کربن (CO2) و متان (CH4) مولکول های غیرقطبی هستند.
اما آیا پیوندهای یونی قطبی نیستند؟
در پیوندهای یونی، الکترون ها در پیوند اساساً به یک اتم از سوی اتم دیگر اهدا می شوند (به عنوان مثال، NaCl). پیوندهای یونی بین اتم ها زمانی شکل می گیرند که تفاوت الکتروگاتیویته بین آن ها بیشتر از 1.7 باشد. از نظر فنی، پیوندهای یونی کاملاً پیوندهای قطبی هستند، بنابراین اصطلاحات ممکن است گیج کننده باشند.
فقط به یاد داشته باشید: پیوند قطبی به نوعی پیوند کووالانسی اشاره دارد که در آن الکترون ها به طور مساوی تقسیم نمی شوند و مقادیر الکتروگاتیویته کمی متفاوت هستند. پیوندهای کووالانسی قطبی بین اتم ها با تفاوت الکتروگاتیویته بین 0.4 و 1.7 تشکیل می شوند.
نمونه های مولکول هایی با پیوندهای کووالانسی قطبی
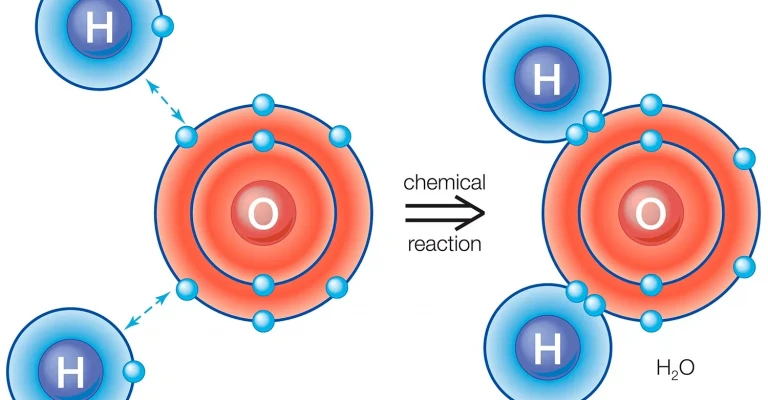
آب (H2O) یک مولکول با پیوند قطبی است. مقدار الکتروگاتیویته اکسیژن 3.44 است، در حالی که الکتروگاتیویته هیدروژن 2.20 است. نابرابری در توزیع الکترون ها شکل خمیده مولکول را توضیح می دهد. "سمت" اکسیژن مولکول دارای بار منفی خالص است، در حالی که دو اتم هیدروژن (در سمت دیگر) دارای بار مثبت خالص هستند.
هیدروژن فلوراید (HF) نمونه ای دیگر از مولکولی است که دارای پیوند کووالانسی قطبی می باشد. در این مولکول، اتم فلورین الکتروگاتیویته بیشتری دارد، بنابراین الکترون های موجود در پیوند بیشتر به اتم فلورین نزدیک هستند تا اتم هیدروژن. در این حالت، یک دیپول شکل می گیرد که سمت فلورین بار منفی خالص و سمت هیدروژن بار مثبت خالص دارد. هیدروژن فلوراید یک مولکول خطی است زیرا تنها دو اتم دارد و بنابراین هیچ هندسه دیگری ممکن نیست.
مولکول آمونیاک (NH3) دارای پیوندهای کووالانسی قطبی بین اتم های نیتروژن و هیدروژن است. در اینجا دیپول به گونه ای است که اتم نیتروژن بار منفی بیشتری دارد و سه اتم هیدروژن همه در یک سمت از اتم نیتروژن با بار مثبت قرار دارند.
کدام عناصر پیوندهای قطبی تشکیل می دهند؟
پیوندهای کووالانسی قطبی بین دو اتم غیرفلزی که الکتروگاتیویته های متفاوتی دارند، تشکیل می شوند. از آنجایی که مقادیر الکتروگاتیویته کمی متفاوت هستند، جفت الکترون های پیوندی به طور مساوی بین اتم ها تقسیم نمی شود. به عنوان مثال، پیوندهای کووالانسی قطبی معمولاً بین هیدروژن و هر غیرفلز دیگری تشکیل می شوند.
مقدار الکتروگاتیویته بین فلزات و غیرفلزات بزرگ است، به همین دلیل آن ها با یکدیگر پیوندهای یونی تشکیل می دهند. هیدروژن معمولاً به عنوان یک غیرفلز عمل می کند نه به عنوان یک فلز.
- شیمی
- علم