ایندیوم (In): خواص، کاربردها و حقایق جالب درباره عنصر شماره 49
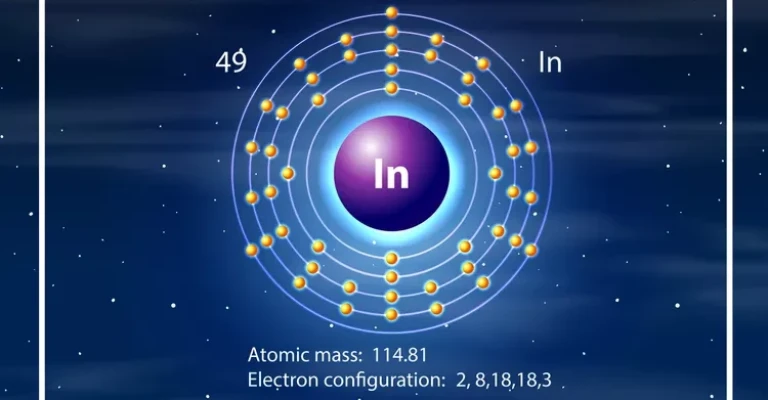
ایندیوم، با نماد شیمیایی In و عدد اتمی 49، یک فلز نقرهای-سفید است که از نظر ظاهری شباهت زیادی به قلع دارد. اما از نظر خواص شیمیایی، بیشتر به گالیم و تالیم نزدیک است.
ایندیوم یکی از نرمترین فلزات شناخته شده است، به طوری که تنها فلزات قلیایی از آن نرمتر هستند. این ویژگی منحصربهفرد، ایندیوم را برای کاربردهای خاصی بسیار مناسب میسازد.
دانستنیهای اساسی درباره ایندیوم
- عدد اتمی: 49
- نماد شیمیایی: In
- وزن اتمی: 114.818
- کاشفان: فردیناند رایش و ت. ریشتر، 1863 (آلمان)
- آرایش الکترونی: [Kr] 5s2 4d10 5p1
- ریشه نام: از کلمه لاتین indicum، به دلیل خط طیفی نیلی درخشان این عنصر.
- ایزوتوپها: 39 ایزوتوپ شناخته شده دارد، با جرم اتمی بین 97 تا 135. تنها یک ایزوتوپ پایدار به صورت طبیعی وجود دارد: In-113. ایزوتوپ طبیعی دیگر، In-115، نیمه عمری برابر با 4.41 x 1014 سال دارد که بسیار بیشتر از عمر جهان است! In-115، 95.7% ایندیوم طبیعی را تشکیل میدهد و باقیمانده آن In-113 است.
- خواص: نقطه ذوب 156.61 °C، نقطه جوش 2080 °C، وزن مخصوص 7.31 (در 20 °C)، ظرفیت 1، 2 یا 3. فلزی بسیار نرم، نقرهای-سفید، با جلای درخشان که هنگام خم شدن صدایی زیر تولید میکند. ایندیوم شیشه را خیس میکند.
- نقش زیستی: ممکن است سمی باشد، اما تحقیقات بیشتری لازم است. هیچ نقش زیستی شناخته شدهای در هیچ ارگانیسمی ندارد. نمکهای ایندیوم(III) برای کلیهها سمی هستند. In-111 رادیواکتیو به عنوان ردیاب رادیویی در پزشکی هستهای برای نشاندار کردن گلبولهای سفید و پروتئینها استفاده میشود. در پوست، ماهیچهها و استخوانها ذخیره میشود، اما تقریباً ظرف دو هفته دفع میگردد.
- کاربردها: در آلیاژهای با نقطه ذوب پایین، آلیاژهای یاتاقان، ترانزیستورها، ترمیستورها، فوتوکانداکتورها و یکسوسازها استفاده میشود. هنگام آبکاری یا تبخیر روی شیشه، آینهای به خوبی نقره ایجاد میکند، اما با مقاومت بالاتری در برابر خوردگی اتمسفری. به آمالگام دندان اضافه میشود تا کشش سطحی جیوه را کاهش داده و به سهولت ترکیب کمک کند. در میلههای کنترل هستهای استفاده میشود. در سال 2009، با منگنز و ایتریوم ترکیب شد تا رنگدانه آبی غیر سمی YInMn blue را تشکیل دهد. میتواند جایگزین جیوه در باتریهای قلیایی شود. به عنوان یک عنصر حیاتی در فناوری در نظر گرفته میشود.
- منابع: اغلب با مواد روی مرتبط است. همچنین در سنگهای آهن، سرب و مس یافت میشود. شصت و هشتمین عنصر فراوان در پوسته زمین است و تقریباً با غلظت 50 قسمت در میلیارد وجود دارد. در فرآیند s در ستارگان کم جرم و متوسط جرم تشکیل شده است. منبع اصلی ایندیوم، اسفالریت است که یک سنگ معدن سولفیدی روی است و به عنوان یک محصول جانبی فرآوری سنگ معدن تولید میشود.
- دستهبندی عنصر: فلز

اطلاعات فیزیکی ایندیوم
- چگالی (g/cc): 7.31
- نقطه ذوب (K): 429.32
- نقطه جوش (K): 2353
- شکل ظاهری: فلز نقرهای-سفید بسیار نرم
- حالات اکسیداسیون: -5, -2, -1, +1, +2, +3
- شعاع اتمی (pm): 166
- حجم اتمی (cc/mol): 15.7
- شعاع کووالانسی (pm): 144
- شعاع یونی: 81 (+3e)
- گرمای ویژه (@20°C J/g mol): 0.234
- گرمای ذوب (kJ/mol): 3.24
- گرمای تبخیر (kJ/mol): 225.1
- دمای دبای (K): 129.00
- عدد الکترونگاتیوی پائولینگ: 1.78
- اولین انرژی یونیزاسیون (kJ/mol): 558.0
- حالات اکسیداسیون: 3
- ساختار شبکه: تتراگونال مرکزدار
- ثابت شبکه (Å): 4.590
- جدول تناوبی
- شیمی
- علم



