الکترونگاتیوی چیست؟ همه چیز درباره جاذبه اتمی برای الکترونها
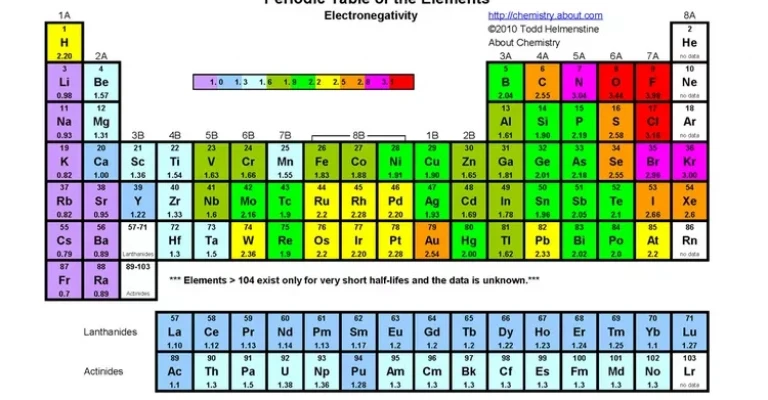
الکترونگاتیوی، که گاهی اوقات به آن الکترونخواهی نیز گفته میشود، به توانایی یک اتم در جذب الکترونهای پیوندی به سمت خود اشاره دارد. در واقع، هرچه یک اتم تمایل بیشتری به جذب الکترونهای موجود در یک پیوند شیمیایی داشته باشد، الکترونگاتیوی آن بالاتر است.
تصور کنید دو اتم با هم پیوند کووالانسی تشکیل دادهاند. اگر الکترونگاتیوی هر دو اتم برابر باشد، الکترونها به طور مساوی بین آنها به اشتراک گذاشته میشوند. اما در بیشتر موارد، یکی از اتمها الکترونگاتیوی بیشتری دارد و در نتیجه، الکترونها را بیشتر به سمت خود میکشد. این موضوع منجر به ایجاد یک پیوند کووالانسی قطبی میشود.
حال اگر اختلاف الکترونگاتیوی بین دو اتم بسیار زیاد باشد، الکترونها دیگر به اشتراک گذاشته نمیشوند. در این حالت، اتم الکترونگاتیوتر، الکترونهای پیوندی را به طور کامل از اتم دیگر میگیرد و پیوند یونی تشکیل میشود.
نکات کلیدی درباره الکترونگاتیوی
- تعریف: الکترونگاتیوی، معیاری از تمایل یک اتم برای جذب الکترونها به سمت خود در یک پیوند شیمیایی است.
- بیشترین و کمترین: فلوئور، با بالاترین مقدار الکترونگاتیوی، قویترین جاذبه را برای الکترونها دارد. فرانسیم، با کمترین مقدار الکترونگاتیوی (یا به عبارت دیگر، بالاترین الکتروپوزیتیوی)، کمترین جاذبه را دارد.
- قطبیت پیوند: هرچه اختلاف الکترونگاتیوی بین دو اتم بیشتر باشد، پیوند شیمیایی تشکیل شده بین آنها قطبیتر خواهد بود.
تاریخچه و مقیاسهای اندازهگیری الکترونگاتیوی
مفهوم الکترونگاتیوی، قبل از نامگذاری رسمی آن توسط یونس یاکوب برزلیوس در سال 1811، توسط آووگادرو و سایر شیمیدانان مورد مطالعه قرار گرفت. در سال 1932، لینوس پاولینگ مقیاسی برای اندازهگیری الکترونگاتیوی بر اساس انرژیهای پیوندی پیشنهاد کرد. مقادیر الکترونگاتیوی در مقیاس پاولینگ اعدادی بدون بعد هستند که بین 0.7 تا 3.98 متغیر هستند. این مقادیر نسبت به الکترونگاتیوی هیدروژن (2.20) سنجیده میشوند.
اگرچه مقیاس پاولینگ پرکاربردترین مقیاس است، مقیاسهای دیگری نیز وجود دارند، از جمله مقیاس مولیکن، مقیاس آلرد-روچو، مقیاس آلن و مقیاس ساندرسون.
عوامل موثر بر الکترونگاتیوی
الکترونگاتیوی، ویژگی یک اتم در داخل یک مولکول است، نه یک ویژگی ذاتی اتم به تنهایی. بنابراین، الکترونگاتیوی در واقع بسته به محیط اطراف اتم متفاوت است. با این حال، در بیشتر موارد، یک اتم رفتار مشابهی در شرایط مختلف از خود نشان میدهد. عواملی که بر الکترونگاتیوی تأثیر میگذارند عبارتند از بار هسته و تعداد و موقعیت الکترونها در یک اتم.
مثالهایی از الکترونگاتیوی در عمل
برای درک بهتر مفهوم الکترونگاتیوی، دو مثال را بررسی میکنیم:
مولکول هیدروژن کلرید (HCl)
اتم کلر، در مقایسه با اتم هیدروژن، الکترونگاتیوی بالاتری دارد. به همین دلیل، الکترونهای پیوندی در مولکول HCl بیشتر به سمت اتم کلر جذب میشوند تا اتم هیدروژن.
مولکول اکسیژن (O2)
در مولکول اکسیژن، هر دو اتم اکسیژن دارای الکترونگاتیوی یکسانی هستند. در نتیجه، الکترونهای موجود در پیوند کووالانسی به طور مساوی بین دو اتم اکسیژن به اشتراک گذاشته میشوند.
الکترونگاتیوترین و الکتروپوزیتیوترین عناصر جدول تناوبی
در جدول تناوبی، فلوئور (با مقدار 3.98) به عنوان الکترونگاتیوترین عنصر شناخته میشود. در مقابل، سزیم (با مقدار 0.79) کمترین میزان الکترونگاتیوی را دارد. به عبارت دیگر، میتوان گفت سزیم، الکتروپوزیتیوترین عنصر جدول است. الکتروپوزیتیوی، مفهومی متضاد با الکترونگاتیوی است.
شایان ذکر است که در منابع قدیمیتر، فرانسیم و سزیم هر دو به عنوان عناصری با کمترین الکترونگاتیوی (مقدار 0.7) ذکر شدهاند. اما مقدار الکترونگاتیوی سزیم به طور تجربی به 0.79 اصلاح شده است. هیچ داده تجربی مستقیمی برای فرانسیم وجود ندارد، اما از آنجا که انرژی یونیزاسیون آن از سزیم بالاتر است، انتظار میرود که فرانسیم کمی الکترونگاتیوتر باشد.
روند الکترونگاتیوی در جدول تناوبی
الکترونگاتیوی، مانند میل الکترونی، شعاع اتمی/یونی و انرژی یونیزاسیون، روند مشخصی را در جدول تناوبی نشان میدهد.
- به طور کلی، الکترونگاتیوی با حرکت از چپ به راست در یک دوره افزایش مییابد. گازهای نجیب معمولاً از این روند مستثنی هستند.
- به طور کلی، الکترونگاتیوی با حرکت به سمت پایین در یک گروه از جدول تناوبی کاهش مییابد. این موضوع با افزایش فاصله بین هسته و الکترونهای لایه ظرفیت مرتبط است.
الکترونگاتیوی و انرژی یونیزاسیون روند مشابهی را در جدول تناوبی دنبال میکنند. عناصری که انرژی یونیزاسیون پایینی دارند، تمایل به داشتن الکترونگاتیوی پایینی نیز دارند. هسته اتم این عناصر، کشش قویای بر روی الکترونها اعمال نمیکند. به طور مشابه، عناصری که انرژی یونیزاسیون بالایی دارند، تمایل به داشتن مقادیر الکترونگاتیوی بالایی دارند. هسته اتم در این عناصر، کشش قویای بر روی الکترونها اعمال میکند.
- شیمی
- علم