نحوه تهیه محلول هیدروکسید سدیم با رعایت نکات ایمنی
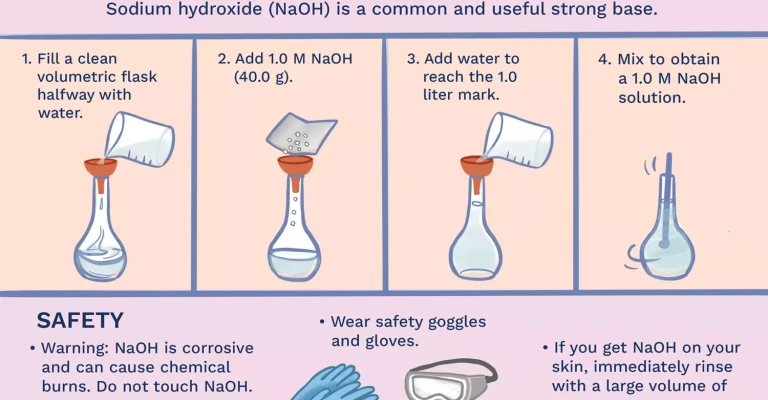
هیدروکسید سدیم یک باز قوی و رایج است که کاربردهای فراوانی دارد. برای تهیه محلول هیدروکسید سدیم یا NaOH در آب، لازم است احتیاط های ویژه ای انجام شود زیرا این واکنش گرمای قابل توجهی ایجاد می کند. ممکن است محلول پاشیده شود یا به جوش بیاید. در اینجا روش ایمن تهیه محلول هیدروکسید سدیم به همراه دستورالعمل هایی برای چند غلظت معمولی محلول NaOH ارائه شده است.
مقدار NaOH برای تهیه محلول هیدروکسید سدیم
محلول های هیدروکسید سدیم را با استفاده از این جدول مرجع تهیه کنید که مقدار جامد (NaOH) لازم برای تهیه 1 لیتر محلول قلیایی را نشان می دهد. دستورات ایمنی آزمایشگاه را رعایت کنید:
- به هیدروکسید سدیم دست نزنید! این ماده سوزاننده است و می تواند باعث سوختگی شیمیایی شود. اگر NaOH روی پوست شما قرار گرفت، فوراً با مقدار زیادی آب آن را بشویید. گزینه دیگر این است که هر باز موجود روی پوست را با یک اسید ضعیف، مانند سرکه خنثی کرده و سپس با آب بشویید.
- هیدروکسید سدیم را به آرامی به مقدار زیادی آب اضافه کنید و سپس محلول را رقیق کنید تا یک لیتر تهیه شود. هیدروکسید سدیم را به آب اضافه کنید - هرگز آب را به هیدروکسید سدیم جامد اضافه نکنید.
- از شیشۀ بوروسیلیکات (مانند Pyrex) استفاده کنید و در نظر داشته باشید که ظرف را در یک سطل یخ غوطه ور کنید تا دما پایین بماند. قبل از استفاده، شیشه ها را بررسی کنید تا از عدم وجود هرگونه ترک، خش یا آسیب جلوگیری شود که نشان دهنده ضعف شیشه باشد. استفاده از شیشه های دیگر یا شیشه های ضعیف ممکن است در تغییر دما باعث شکستن آن شود.
- عینک ایمنی و دستکش بپوشید زیرا ممکن است محلول هیدروکسید سدیم به اطراف پاشیده شود یا شیشه بشکند. محلول های غلیظ هیدروکسید سدیم خورنده هستند و باید با احتیاط استفاده شوند.
دستورالعمل های تهیه محلول های رایج NaOH
برای تهیه این دستورالعمل ها، با 1 لیتر آب شروع کنید و به آرامی جامد NaOH را هم بزنید. اگر بار مغناطیسی دارید، استفاده از آن مفید خواهد بود.
- شیمی
- علم



