لیست اسیدهای قوی و ضعیف: شناخت و تفاوت ها
اسیدها نقش مهمی در علم شیمی و کاربردهای عملی آن ایفا می کنند. شناخت اسیدهای قوی و ضعیف نه تنها برای درک مفاهیم پایه ای شیمی ضروری است، بلکه در آزمایشگاه ها و صنایع مختلف نیز کاربردهای گسترده ای دارد. اسیدهای قوی به طور کامل در آب تفکیک می شوند و یون های خود را آزاد می کنند، در حالی که اسیدهای ضعیف تنها بخشی از مولکول های خود را تفکیک می کنند. در این مطلب، به بررسی تفاوت های این دو نوع اسید، لیستی از اسیدهای قوی و ضعیف رایج، و روش های تشخیص آن ها می پردازیم.
تفاوت اسیدهای قوی و ضعیف
اسیدهای قوی و ضعیف از نظر میزان تفکیک یا یونیزاسیون در آب با یکدیگر تفاوت دارند. اسیدهای قوی به طور کامل در آب تفکیک می شوند و تمام مولکول های آن ها به یون های مثبت (هیدروژن) و منفی تبدیل می شوند. این فرآیند باعث می شود که غلظت یون های هیدروژن در محلول به طور قابل توجهی افزایش یابد. از طرفی، اسیدهای ضعیف تنها بخشی از مولکول های خود را در آب تفکیک می کنند و تعادلی بین مولکول های تفکیک شده و تفکیک نشده برقرار می شود. این تفاوت در میزان تفکیک، تأثیر مستقیمی بر قدرت اسیدی و رفتار شیمیایی آن ها دارد.
به عنوان مثال، اسید کلریدریک (HCl) یک اسید قوی است که به طور کامل به یون های هیدروژن و کلرید تفکیک می شود، در حالی که اسید استیک (CH3COOH) یک اسید ضعیف است که تنها بخش کوچکی از مولکول های آن در آب تفکیک می شوند. این تفاوت ها باعث می شود که اسیدهای قوی در واکنش های شیمیایی سریع تر و قوی تر عمل کنند، در حالی که اسیدهای ضعیف واکنش های ملایم تری دارند.
لیست اسیدهای قوی رایج
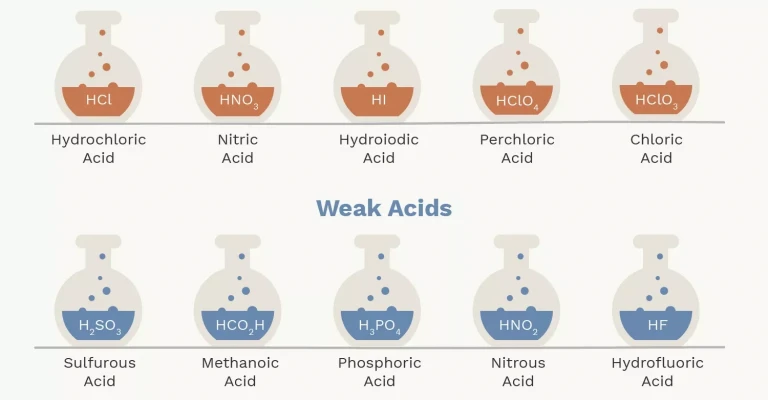
اسیدهای قوی به اسیدهایی گفته می شوند که در آب به طور کامل تفکیک می شوند و تمام مولکول های آن ها به یون های مثبت و منفی تبدیل می شوند. این ویژگی باعث می شود که اسیدهای قوی قدرت اسیدی بسیار بالایی داشته باشند. در طبیعت، تنها تعداد محدودی از اسیدها به عنوان اسیدهای قوی شناخته می شوند. در زیر لیستی از هفت اسید قوی رایج آورده شده است:
- HCl - اسید کلریدریک (هیدروکلریک اسید)
- HNO3 - اسید نیتریک
- H2SO4 - اسید سولفوریک (البته یون HSO4- یک اسید ضعیف است)
- HBr - اسید هیدروبرمیک
- HI - اسید هیدرویدیک
- HClO4 - اسید پرکلریک
- HClO3 - اسید کلریک
به عنوان مثال، واکنش تفکیک اسید کلریدریک در آب به صورت زیر است:
HCl → H+ + Cl-
در این واکنش، تمام مولکول های HCl به یون های هیدروژن و کلرید تفکیک می شوند و هیچ مولکول تفکیک نشده ای در محلول باقی نمی ماند. این ویژگی باعث می شود که اسیدهای قوی در واکنش های شیمیایی بسیار مؤثر و قوی عمل کنند.
لیست اسیدهای ضعیف رایج
اسیدهای ضعیف به اسیدهایی گفته می شوند که در آب به طور کامل تفکیک نمی شوند و تنها بخشی از مولکول های آن ها به یون های مثبت و منفی تبدیل می شوند. این ویژگی باعث می شود که اسیدهای ضعیف قدرت اسیدی کمتری نسبت به اسیدهای قوی داشته باشند. تعداد اسیدهای ضعیف بسیار بیشتر از اسیدهای قوی است و بسیاری از اسیدهای آلی در این دسته قرار می گیرند. در زیر لیستی از برخی اسیدهای ضعیف رایج آورده شده است:
- HO2C2O2H - اسید اگزالیک
- H2SO3 - اسید سولفورو
- HSO4- - یون هیدروژن سولفات
- H3PO4 - اسید فسفریک
- HNO2 - اسید نیترو
- HF - اسید هیدروفلوئوریک
- HCO2H - اسید متانوئیک (فرمیک اسید)
- C6H5COOH - اسید بنزوئیک
- CH3COOH - اسید استیک
- HCOOH - اسید فرمیک
به عنوان مثال، واکنش تفکیک اسید استیک در آب به صورت زیر است:
CH3COOH + H2O ⇆ H3O+ + CH3COO-
در این واکنش، تنها حدود ۱٪ از مولکول های اسید استیک به یون های هیدروژن و استات تفکیک می شوند و بقیه به صورت مولکول های تفکیک نشده باقی می مانند. این تعادل بین مولکول های تفکیک شده و تفکیک نشده باعث می شود که اسیدهای ضعیف واکنش های شیمیایی ملایم تری داشته باشند.
تشخیص اسیدهای قوی و ضعیف با استفاده از ثابت تعادل
یکی از روش های علمی برای تشخیص اسیدهای قوی و ضعیف، استفاده از ثابت تعادل اسید (Ka) یا لگاریتم منفی آن (pKa) است. ثابت تعادل اسید (Ka) نشان دهنده میزان تمایل اسید به تفکیک در آب و آزاد کردن یون های هیدروژن است. هرچه مقدار Ka بزرگ تر باشد، اسید قوی تر است و برعکس، هرچه Ka کوچک تر باشد، اسید ضعیف تر است.
به طور کلی، اسیدهای قوی دارای مقادیر Ka بسیار بالا یا pKa بسیار پایین هستند، در حالی که اسیدهای ضعیف دارای مقادیر Ka بسیار کوچک یا pKa بالا هستند. برای مثال، اسید کلریدریک (HCl) یک اسید قوی است و مقدار Ka آن بسیار بالا است، در حالی که اسید استیک (CH3COOH) یک اسید ضعیف است و مقدار Ka آن بسیار کوچک است.
با استفاده از این مقادیر، می توان به راحتی قدرت اسیدی یک ماده را ارزیابی کرد. به عنوان مثال، اگر مقدار pKa یک اسید کمتر از ۱ باشد، معمولاً آن اسید در دسته اسیدهای قوی قرار می گیرد، در حالی که مقادیر pKa بالاتر از ۴ نشان دهنده اسیدهای ضعیف هستند.
این روش نه تنها در آزمایشگاه های شیمی کاربرد دارد، بلکه در صنایع مختلف مانند داروسازی و تولید مواد شیمیایی نیز برای انتخاب اسیدهای مناسب استفاده می شود.
تفاوت اسیدهای قوی و ضعیف با اسیدهای غلیظ و رقیق
مفهوم قدرت اسیدی (قوی یا ضعیف بودن) با غلظت اسید (غلیظ یا رقیق بودن) متفاوت است و این دو اصطلاح نباید با یکدیگر اشتباه گرفته شوند. قدرت اسیدی به میزان تفکیک اسید در آب و آزاد کردن یون های هیدروژن اشاره دارد، در حالی که غلظت اسید به مقدار اسید موجود در یک حجم مشخص از محلول مربوط می شود.
یک اسید قوی مانند اسید کلریدریک (HCl) حتی در غلظت های بسیار پایین نیز به طور کامل تفکیک می شود و قدرت اسیدی بالایی دارد. از طرفی، یک اسید ضعیف مانند اسید استیک (CH3COOH) حتی در غلظت های بالا نیز تنها بخشی از مولکول های خود را تفکیک می کند و قدرت اسیدی کمتری دارد.
به عنوان مثال، محلولی از اسید استیک با غلظت ۱۲ مول بر لیتر، یک اسید غلیظ است اما همچنان یک اسید ضعیف محسوب می شود. برعکس، محلولی از اسید کلریدریک با غلظت ۰٫۰۰۰۵ مول بر لیتر، یک اسید رقیق است اما همچنان یک اسید قوی به شمار می آید.
بنابراین، غلظت اسید نشان دهنده مقدار اسید در محلول است، در حالی که قدرت اسیدی نشان دهنده توانایی اسید در تفکیک و آزاد کردن یون های هیدروژن است. این تفاوت ها در کاربردهای عملی شیمی و صنعت بسیار مهم هستند و باید به دقت مورد توجه قرار گیرند.
اسیدهای قوی در مقابل اسیدهای خورنده
اسیدهای قوی و اسیدهای خورنده دو مفهوم متفاوت هستند که گاهی با یکدیگر اشتباه گرفته می شوند. اسیدهای قوی به اسیدهایی گفته می شوند که به طور کامل در آب تفکیک می شوند و یون های هیدروژن آزاد می کنند، در حالی که اسیدهای خورنده به اسیدهایی اطلاق می شوند که توانایی آسیب رساندن به بافت های زنده یا مواد دیگر را دارند. این دو ویژگی لزوماً با هم مرتبط نیستند.
به عنوان مثال، اسید سولفوریک (H2SO4) یک اسید قوی و بسیار خورنده است که می تواند باعث سوختگی شیمیایی شدید شود. از طرفی، اسید استیک (CH3COOH) که یک اسید ضعیف است، در غلظت های پایین (مانند سرکه) بی خطر است و حتی قابل مصرف است. با این حال، برخی اسیدهای ضعیف مانند اسید هیدروفلوئوریک (HF) نیز بسیار خورنده هستند و می توانند به بافت های عمیق بدن نفوذ کنند.
جالب توجه است که برخی از قوی ترین اسیدهای شناخته شده، مانند اسیدهای سوپراسید (مانند کربوران ها)، به رغم قدرت اسیدی بسیار بالا، خورندگی کمی دارند و حتی می توان آن ها را در دست نگه داشت. این موضوع نشان می دهد که قدرت اسیدی و خورندگی لزوماً به یکدیگر وابسته نیستند و هر کدام ویژگی های خاص خود را دارند.
بنابراین، هنگام کار با اسیدها، باید هم به قدرت اسیدی و هم به خورندگی آن ها توجه کرد تا از خطرات احتمالی جلوگیری شود.
- شیمی
- علم



