مدل اتمی بور: بررسی و ویژگی ها
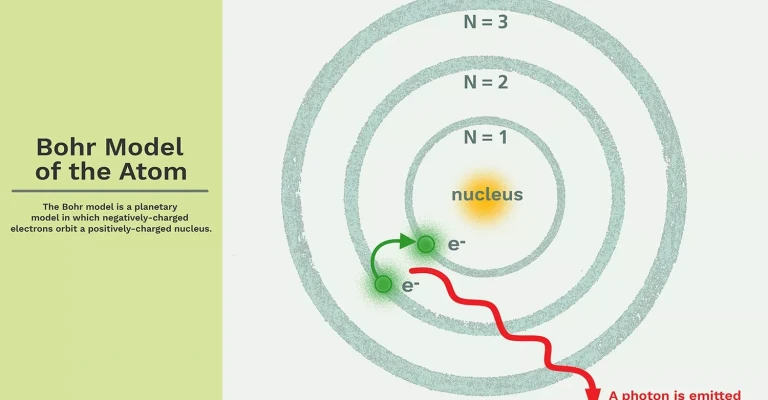
مدل بور یک مدل اتمی است که در آن هسته ای کوچک و دارای بار مثبت وجود دارد و الکترون های دارای بار منفی به دور آن در حال گردش هستند. در اینجا نگاهی دقیق تر به این مدل سیاره ای داریم.
بررسی اجمالی مدل بور
نیلز بور در سال ۱۹۱۵ مدل بور اتم را پیشنهاد داد. از آنجا که مدل بور تغییراتی از مدل قبلی رادرفورد است، برخی به مدل بور، مدل رادرفورد-بور می گویند. مدل مدرن اتم مبتنی بر مکانیک کوانتومی است. مدل بور دارای برخی اشتباهات است، اما به دلیل توصیف ویژگی های پذیرفته شده نظریه اتم بدون استفاده از ریاضیات پیچیده مدل مدرن، اهمیت دارد. بر خلاف مدل های قبلی، مدل بور فرمول ریدبرگ برای خطوط انتشار طیفی هیدروژن اتمی را توضیح می دهد.
مدل بور یک مدل سیاره ای است که در آن الکترون های دارای بار منفی به دور هسته کوچک و دارای بار مثبت می چرخند، مشابه سیاراتی که به دور خورشید می چرخند (مگر اینکه مدارها صفحه ای نباشند). نیروی گرانش سیستم خورشیدی به طور ریاضی شبیه به نیروی کولن (الکتریکی) بین هسته دارای بار مثبت و الکترون های دارای بار منفی است.
- الکترون ها در مداراتی با اندازه و انرژی معین به دور هسته می چرخند.
- انرژی مدار با اندازه آن مرتبط است. کمترین انرژی در کوچک ترین مدار یافت می شود.
- هنگامی که یک الکترون از یک مدار به مدار دیگر حرکت می کند، تابش انرژی جذب یا منتشر می شود.
مدل بور برای هیدروژن
ساده ترین مثال از مدل بور برای اتم هیدروژن (Z = 1) یا برای یک یون شبیه هیدروژن (Z > 1) است، که در آن یک الکترون دارای بار منفی به دور هسته ای کوچک و دارای بار مثبت می چرخد. انرژی الکترومغناطیسی در صورت حرکت یک الکترون از یک مدار به مدار دیگر جذب یا منتشر می شود. تنها مدارهای خاصی برای الکترون ها مجاز هستند. شعاع مدارهای مجاز به صورت n² افزایش می یابد، جایی که n شماره کوانتومی اصلی است. انتقال 3 → 2 اولین خط از سری بالمر را تولید می کند. برای هیدروژن (Z = 1) این یک فوتون با طول موج ۶۵۶ نانومتر (نور قرمز) تولید می کند.
مدل بور برای اتم های سنگین تر
اتم های سنگین تر پروتون های بیشتری در هسته نسبت به اتم هیدروژن دارند. الکترون های بیشتری برای خنثی کردن بار مثبت تمام پروتون ها لازم است. بور بر این باور بود که هر مدار الکترون تنها می تواند تعداد معینی از الکترون ها را نگه دارد. هنگامی که سطح پر می شود، الکترون های اضافی به سطح بعدی منتقل می شوند. بنابراین، مدل بور برای اتم های سنگین تر، پوسته های الکترونی را توصیف کرد. این مدل برخی از خواص اتمی اتم های سنگین تر را که قبلاً هرگز تولید نشده بودند، توضیح داد. به عنوان مثال، مدل پوسته ای توضیح می دهد که چرا اتم ها در حین حرکت در یک دوره (ردیف) از جدول تناوبی کوچکتر می شوند، حتی اگر پروتون ها و الکترون های بیشتری داشته باشند. همچنین توضیح می دهد که چرا گازهای نجیب غیر فعالند و چرا اتم های سمت چپ جدول تناوبی الکترون ها را جذب می کنند، در حالی که اتم های سمت راست آن ها را از دست می دهند. با این حال، این مدل فرض می کند که الکترون ها در پوسته ها با یکدیگر تعامل ندارند و نمی تواند توضیح دهد که چرا الکترون ها به نظر می رسد به طور نامنظم انباشته می شوند.
مشکلات مدل بور
- این مدل با اصل عدم قطعیت هایزنبرگ تناقض دارد زیرا الکترون ها را به عنوان موجوداتی با شعاع و مداری مشخص در نظر می گیرد.
- مدل بور ارزش نادرستی برای مومنتم زاویه ای مدار حالت پایه ارائه می دهد.
- این مدل پیش بینی های ضعیفی در مورد طیف های اتم های بزرگ تر دارد.
- مدل بور نمی تواند شدت های نسبی خطوط طیفی را پیش بینی کند.
- این مدل ساختار ظریف و ساختار فوق ظریف در خطوط طیفی را توضیح نمی دهد.
- مدل بور اثر زیمان را توضیح نمی دهد.
اصلاحات و بهبودها در مدل بور
مشهورترین اصلاح در مدل بور، مدل زمرفلد است که گاهی به آن مدل بور-زمرفلد می گویند. در این مدل، الکترون ها در مسیرهای بیضوی به دور هسته حرکت می کنند نه در مسیرهای دایره ای. مدل زمرفلد در توضیح اثرات طیفی اتمی، مانند اثر استارک در تقسیم خطوط طیفی، بهتر عمل کرد. با این حال، این مدل نمی توانست شماره کوانتومی مغناطیسی را در نظر بگیرد.
در نهایت، مدل بور و مدل های مبتنی بر آن در سال ۱۹۲۵ با مدل ولفگانگ پائولی که بر اساس مکانیک کوانتومی بود، جایگزین شدند. این مدل برای تولید مدل مدرن که توسط اروین شرودینگر در ۱۹۲۶ معرفی شد، بهبود یافت. امروزه رفتار اتم هیدروژن با استفاده از مکانیک موجی برای توصیف مدارهای اتمی توضیح داده می شود.
- شیمی
- علم



