تفاوت بین جرم اتمی و عدد جرمی در شیمی
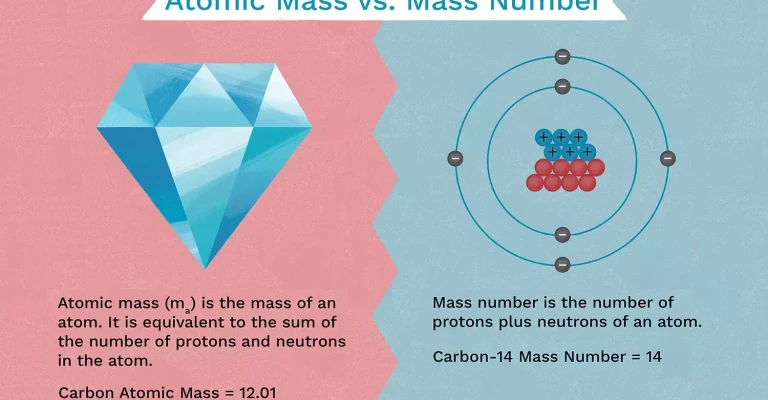
در شیمی، تفاوت بین جرم اتمی و عدد جرمی وجود دارد. جرم اتمی وزن میانگین یک عنصر است، در حالی که عدد جرمی مجموع تعداد نوکلئون ها در هسته اتم می باشد.
- جرم اتمی به عنوان وزن اتمی شناخته می شود و عبارت است از وزن میانگین یک اتم از یک عنصر که بر اساس فراوانی طبیعی نسبی ایزوتوپ های آن عنصر محاسبه می شود.
- عدد جرمی تعداد کل پروتون ها و نوترون ها در هسته اتم است.
نکات کلیدی
- عدد جرمی مجموع تعداد پروتون ها و نوترون ها در یک اتم است و این یک عدد صحیح می باشد.
- جرم اتمی میانگین تعداد پروتون ها و نوترون ها برای تمامی ایزوتوپ های طبیعی یک عنصر است و این یک عدد اعشاری است.
- مقدار جرم اتمی ممکن است گاهی اوقات در طول زمان در نشریات تغییر کند زیرا دانشمندان محاسبات مربوط به فراوانی ایزوتوپ های طبیعی عناصر را اصلاح می کنند.
مثال جرم اتمی و عدد جرمی
هیدروژن دارای سه ایزوتوپ طبیعی است: 1H، 2H و 3H. هر ایزوتوپ عدد جرمی متفاوتی دارد.
1H دارای 1 پروتون است و عدد جرمی آن 1 است. 2H دارای 1 پروتون و 1 نوترون است و عدد جرمی آن 2 می باشد. 3H نیز دارای 1 پروتون و 2 نوترون است و عدد جرمی آن 3 است. 99.98% از تمام هیدروژن، 1H است. این با 2H و 3H ترکیب می شود تا مقدار کل جرم اتمی هیدروژن را به وجود آورد که معادل 1.00784 g/mol است.
عدد اتمی و عدد جرمی
مراقب باشید که عدد اتمی و عدد جرمی را اشتباه نگیرید. در حالی که عدد جرمی مجموع پروتون ها و نوترون ها در یک اتم است، عدد اتمی فقط تعداد پروتون ها را نشان می دهد. عدد اتمی مقداری است که با یک عنصر در جدول تناوبی مرتبط است و کلید شناسایی عنصر می باشد. تنها زمانی که عدد اتمی و عدد جرمی یکسان است، زمانی است که با ایزوتوپ پروتیوم هیدروژن سروکار داریم که تنها شامل یک پروتون است. هنگامی که به عناصر به طور کلی فکر می کنید، به خاطر داشته باشید که عدد اتمی هرگز تغییر نمی کند، اما ممکن است به دلیل وجود چندین ایزوتوپ، عدد جرمی تغییر کند.
- شیمی
- علم



