اسید آمینه چیست؟ تعریف، عملکردها، انواع و مثالها
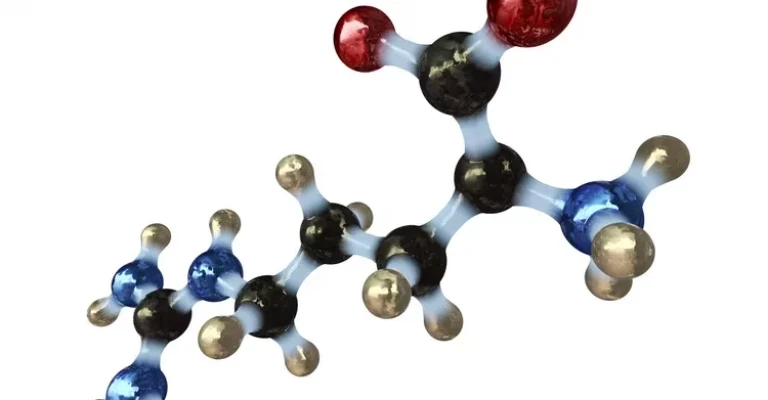
اسیدهای آمینه نقش حیاتی در زیستشناسی، بیوشیمی و پزشکی ایفا میکنند. آنها به عنوان بلوکهای سازنده پلیپپتیدها و پروتئینها شناخته میشوند، مولکولهایی که ساختار و عملکرد سلولها را تعیین میکنند.
در این مطلب، به بررسی ترکیبات شیمیایی، عملکردهای متنوع، اختصارات و ویژگیهای منحصربهفرد اسیدهای آمینه میپردازیم.
اسید آمینه چیست؟
- اسید آمینه یک ترکیب آلی است که دارای یک گروه کربوکسیل (-COOH)، یک گروه آمینه (-NH2) و یک زنجیره جانبی (R) متصل به یک اتم کربن مرکزی است. این زنجیره جانبی، هویت و خواص منحصر به فرد هر اسید آمینه را تعیین میکند.
- اسیدهای آمینه پیشساز سایر مولکولهای مهم در بدن هستند. اتصال اسیدهای آمینه به یکدیگر، پلیپپتیدها را تشکیل میدهد که میتوانند به پروتئین تبدیل شوند.
- اسیدهای آمینه از طریق کد ژنتیکی در ریبوزومهای سلولهای یوکاریوتی ساخته میشوند.
- کد ژنتیکی، دستورالعملی برای ساخت پروتئینها در سلول است. DNA به RNA ترجمه میشود و سپس سه باز (ترکیبی از آدنین، اوراسیل، گوانین و سیتوزین) یک اسید آمینه را رمزگذاری میکنند. برای هر اسید آمینه معمولاً بیش از یک کد وجود دارد.
- برخی از اسیدهای آمینه توسط بدن انسان قابل تولید نیستند. این اسیدهای آمینه "ضروری" باید از طریق رژیم غذایی تامین شوند.
- علاوه بر این، فرآیندهای متابولیکی دیگر، مولکولها را به اسیدهای آمینه تبدیل میکنند.
تعریف اسید آمینه
اسید آمینه نوعی اسید آلی است که شامل یک گروه عاملی کربوکسیل (-COOH)، یک گروه عاملی آمین (-NH2) و یک زنجیره جانبی (R) است که برای هر اسید آمینه منحصربهفرد است. تمام اسیدهای آمینه حاوی عناصر کربن، هیدروژن، اکسیژن و نیتروژن هستند، اما زنجیرههای جانبی آنها ممکن است حاوی عناصر دیگری نیز باشند.
برای نمایش اسیدهای آمینه میتوان از اختصارات سهحرفی یا تکحرفی استفاده کرد. به عنوان مثال، والین را میتوان با V یا val نشان داد و هیستیدین را با H یا his.
اسیدهای آمینه ممکن است به تنهایی عمل کنند، اما بیشتر به عنوان مونومر برای تشکیل مولکولهای بزرگتر عمل میکنند. اتصال چند اسید آمینه به یکدیگر پپتیدها را تشکیل میدهد و زنجیرهای از اسیدهای آمینه، پلیپپتید نامیده میشود. پلیپپتیدها ممکن است تغییر کرده و با هم ترکیب شوند تا پروتئینها را تشکیل دهند.
ساخت پروتئین
فرآیند تولید پروتئین بر اساس یک الگوی RNA، ترجمه نامیده میشود و در ریبوزومهای سلولها رخ میدهد. ۲۲ اسید آمینه در تولید پروتئین نقش دارند که پروتئینزا در نظر گرفته میشوند. علاوه بر اسیدهای آمینه پروتئینزا، برخی اسیدهای آمینه وجود دارند که در هیچ پروتئینی یافت نمیشوند. به عنوان مثال، انتقالدهنده عصبی گاما آمینوبوتیریک اسید (GABA). به طور معمول، اسیدهای آمینه غیر پروتئینزا در متابولیسم اسیدهای آمینه نقش دارند.
ترجمه کد ژنتیکی شامل ۲۰ اسید آمینه است که اسیدهای آمینه کانونی یا استاندارد نامیده میشوند. برای هر اسید آمینه، یک سری از سه باقیمانده mRNA به عنوان یک کدون در طول ترجمه (کد ژنتیکی) عمل میکند. دو اسید آمینه دیگر موجود در پروتئینها پیرولیزین و سلنوسیستئین هستند که به طور ویژهای کدگذاری شدهاند، معمولاً توسط یک کدون mRNA که در غیر این صورت به عنوان یک کدون پایان عمل میکند.
اشتباهات املایی رایج: ammino acid
نمونههایی از اسیدهای آمینه: لیزین، گلیسین، تریپتوفان
نقشهای اسیدهای آمینه در بدن
از آنجا که اسیدهای آمینه برای ساخت پروتئینها استفاده میشوند، بیشتر بدن انسان از آنها تشکیل شده است. فراوانی آنها در بدن، پس از آب در رتبه دوم قرار دارد. اسیدهای آمینه در ساخت انواع مولکولها و انتقالدهندههای عصبی و چربیها نقش دارند.
کایرالیته اسیدهای آمینه
اسیدهای آمینه خاصیت کایرالیته دارند، به این معنی که گروههای عاملی آنها میتوانند در هر طرف پیوند C-C قرار گیرند. در طبیعت، بیشتر اسیدهای آمینه از نوع L-ایزومر هستند. موارد کمی از D-ایزومر نیز وجود دارد. به عنوان مثال، پلیپپتید گرامیسیدین از مخلوطی از D- و L-ایزومرها تشکیل شده است.
اختصارات یک حرفی و سه حرفی اسیدهای آمینه
اسیدهای آمینهای که بیشتر در بیوشیمی به خاطر سپرده میشوند و با آنها مواجه میشویم عبارتند از:
- گلیسین، Gly، G
- والین، Val، V
- لوسین، Leu، L
- ایزولوسین، Ile، I
- پرولین، Pro، P
- ترئونین، Thr، T
- سیستئین، Cys، C
- متیونین، Met، M
- فنیلآلانین، Phe، F
- تیروزین، Tyr، Y
- تریپتوفان، Trp، W
- آرژنین، Arg، R
- آسپارتات، Asp، D
- گلوتامات، Glu، E
- آسپاراژین، Asn، N
- گلوتامین، Gln، Q
- آسپاراژین، Asn، N
ویژگیهای اسیدهای آمینه
ویژگیهای اسیدهای آمینه به ترکیب زنجیره جانبی R آنها بستگی دارد. با استفاده از اختصارات تکحرفی:
- قطبی یا آبدوست (هیدروفیلیک): N, Q, S, T, K, R, H, D, E
- غیرقطبی یا آبگریز (هیدروفوبیک): A, V, L, I, P, Y, F, M, C
- حاوی گوگرد: C, M
- پیوند هیدروژنی: C, W, N, Q, S, T, Y, K, R, H, D, E
- یونیزهشدنی: D, E, H, C, Y, K, R
- حلقوی: P
- آروماتیک: F, W, Y (H نیز هست، اما جذب UV زیادی نشان نمیدهد)
- آلیفاتیک: G, A, V, L, I, P
- تشکیل پیوند دیسولفیدی: C
- اسیدی (دارای بار مثبت در pH خنثی): D, E
- بازی (دارای بار منفی در pH خنثی): K, R
- شیمی
- علم